в корзину
Корзина покупокДЕТАЛЬНО ИЗУЧЕНА КРИСТАЛЛИЧЕСКАЯ СТРУКТУРА КАРБОНАТА АММОНИЯ
ДЕТАЛЬНО ИЗУЧЕНА КРИСТАЛЛИЧЕСКАЯ СТРУКТУРА КАРБОНАТА АММОНИЯ
Результаты новых изучений структуры, казалось бы, простого вещества – моногидрата карбоната аммония – могут оказаться полезными для создания новых и модификации существующих промышленных процессов, позволят ответить на некоторые вопросы, касающиеся биохимии и даже межзвездного формирования строительных блоков живой ткани.
Для установления точной кристаллической структуры моногидрата карбоната аммония исследователи из Испании и Великобритании использовали методы дифракционного исследования монокристаллов совместно с импульсным нейтронным излучением при 10 и 100 Кельвинах. Полученные результаты были соотнесены с результатами порошкового рентгена, полученными в интервале 245-273 K, спектрами комбинационного рассеивания (80-263 K), фононными спектрами, а также результатами расчета электронной конфигурации (NH4)2CO3˙H2O методами DFT.
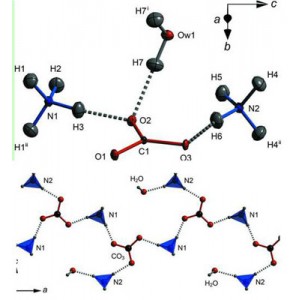
Кристаллическая структура моногидрата карбоната аммония (сверху); мотив формирования кристаллической решетки моногидрата карбоната аммония (снизу). (Рисунок из Acta Crystallographica Section B Structural Science, Crystal Engineering and Materials, 2014; 70 (6): 948)
Внешне простые вещества молекулярного и ионного строения привлекают фундаментальный интерес специалистов по кристаллографии, в первую очередь тем, что относительно простая структура и сравнительно небольшое количество атомов делает их удобными моделями для детального исследования кристаллической структуры, а также снижает объем данных, которые должны быть переработаны при их компьютерном моделировании.
Одним из таких соединений является моногидрат карбоната аммония – (NH4)2CO3˙H2O , который был впервые описан еще в 1800 году Сэром Хемфри Дэви. Несмотря на большую историю и кажущуюся простоту (NH4)2CO3˙H2O до сих пор остается в некотором роде загадочным веществом: такие свойства соединения, как особенности его термического расширения и топологию водородных связей тяжело, если не невозможно, адекватно описать на теоретическом уровне.
Доминик Форте (Dominic Fortes) из Университета Лондона с коллегами из Великобритании и Испании изучил (NH4)2CO3˙H2O, вещество, образующееся в простой тройной системе диоксид углерода/аммиак/вода. Тройка этих реагентов часто может появляться совместно как в промышленных процессах, так и во многих биохимических реакциях.
Будучи кристаллическим материалом, (NH4)2CO3˙H2O существует в различных формах, и с момента его открытия публиковались противоречащие друг другу сообщения о точном составе этого вещества в твердом состоянии. Способность вещества образовывать различные кристаллические фазы привела к тому, что сравнительно недавно – в 1992 году – у ряда исследователей возникал вопрос о том, насколько справедлива формула, приводящаяся для коммерчески реализуемого моногидрата карбоната аммония (правда, этот вопрос отчасти был вынесен на повестку дня еще и потому, что в один из поставщиков реагентов в упаковках, маркированных «карбонат аммония» отгрузил потребителю карбамата того же аммония).
Результаты, полученные Форте, позволяют говорить об установлении точной кристаллической структуры моногидрата карбоната аммония. Исследователи сообщают о том, что в интервале 10-273 К не происходит никаких фазовых переходов этого вещества, однако при температуре выше 273 К моногидрат карбоната аммония первоначально переходит в моногидрат сесквикарбоната аммония, а затем – в бикарбонат аммония.
Химические родственники в основном безвредного моногидрата карбоната аммония, включая токсичный оксалат аммония и взрывоопасный хлорат аммония, изучены гораздо лучше, несмотря на гораздо более редкое их использование в качестве лабораторных материалов. Форте считает любопытным тот факт, что к свойствам и структуре (NH4)2CO3˙H2O интерес практически не проявлялся. Заполнить пробел в знаниях о моногидрате карбоната аммония интересно еще и потому, что вода, углекислый газ и аммиак – довольно распространённые компоненты межзвездного, кометного и планетарного льда, поэтому (NH4)2CO3˙H2O мог сыграть свою роль в процессах химической эволюции вплоть до формирования строительных блоков живых систем, как на Земле, так и, возможно, еще где-нибудь во Вселенной.
Форте добавляет, что дальнейшие планы исследователей заключаются в изменении физических свойств (NH4)2CO3˙H2O и родственных соединений. Уже запланированы эксперименты с карбонатом аммония при высоком давлении – эти эксперименты позволят определить степень сжимаемости вещества, и, возможно, помогут в обнаружении новых полиморфных модификаций этого вещества, образующихся при высоком давлении.
Источник: Acta Crystallographica Section B Structural Science, Crystal Engineering and Materials, 2014; 70 (6): 948 DOI: 10.1107/S205252061402126X
О КОМПАНИИ
 ЗАО "Союзхимпром" более 15 лет работает в области комплексного оснащения химических и эколого-аналитических лабораторий, предприятий разного профиля, государственных служб охраны окружающей среды и санитарного контроля Урала, Сибири и Дальнего Востока.Все что Вам нужно. Основное преимущество новосибирского ЗАО "Союзхимпром" — комплексность поставки.
ЗАО "Союзхимпром" более 15 лет работает в области комплексного оснащения химических и эколого-аналитических лабораторий, предприятий разного профиля, государственных служб охраны окружающей среды и санитарного контроля Урала, Сибири и Дальнего Востока.Все что Вам нужно. Основное преимущество новосибирского ЗАО "Союзхимпром" — комплексность поставки.
КОНТАКТЫ
- 8-383-289-98-09; 289-98-08; 279-98-76; 279-97-52
- info.shp@yandex.ru
- shp-nsk
- 630015, Россия, Новосибирск, ул. Королева 40, корпус 87
Союзхимпром - лабораторное оборудование © 2024