в корзину
Корзина покупокВ ВОДНЫХ РАСТВОРАХ СИЛЬНЫХ КИСЛОТ ИОНЫ БЛИЖЕ, ЧЕМ СЧИТАЛОСЬ
В ВОДНЫХ РАСТВОРАХ СИЛЬНЫХ КИСЛОТ ИОНЫ БЛИЖЕ, ЧЕМ СЧИТАЛОСЬ
Более глубокое понимание особенностей протекания кислотно-основных взаимодействий могут оказаться полезными для оптимизации огромного количества технологий – от нефтедобычи и нефтепереработки до ионных аккумуляторов.
В новой работе исследователи обнаружили, что в водных растворах сильных кислот, например, хлороводородной кислоты (HCl), отрицательно заряженный анион и гидроксоний-катион остаются сближенными, формируя необычную структуру. Такие результаты позволяют добиться более эффективного понимания сложности кислотно-основных процессов, протекающих в концентрированных, не идеальных растворах.
Результаты нового исследования, проясняющие роль противоиона (хлорид-аниона в случае HCl) в растворах, проявляющих сильнокислые свойства, позволяет построить модель, в которой связываются строение кислоты и свойства ее раствора. Такая модель может оказаться полезной для исследователей для еще большей детализации представлений самых основных концепций химии, которая, например, может быть использована для получения фундаментальной информации, необходимой в изучении химии кислотных аккумуляторов.
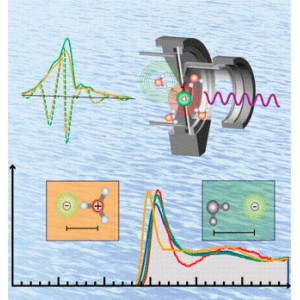
Рисунок из The Journal of Physical Chemistry B, 2014; 118 (26): 7211
В школьных учебниках по химии написано, что при растворении сильной кислоты в воде происходит быстрая диссоциация кислоты и ионы быстро «разбегаются» в разные стороны – все это верно для тех примеров водных растворов, в которых мы имеем дело с низкой концентрации кислоты. Тем не менее, по умолчанию предполагалось, что аналогичная ситуация характерна и для концентрированных растворов. Так, для раствора соляной (хлороводородной кислоты) предполагалось, что образовавшиеся в результате диссоциации ионы H+ быстро диффундируют по раствору, обеспечивая его кислую среду, нейтрализуя основные соединения, вызывая коррозию металлов и/или взаимодействуя с органическими соединениями, в конце концов, взаимодействуя с водой, образуя ион гидроксония H3O+, в то время как анион (Cl–) образует независимые отрицательно заряженные сольво-ассоциаты.
Тем не менее, фундаментальные свойства анионов, окруженных молекулами воды, не были изучены экспериментально в должной степени. В новой работе исследователи, используя методы компьютерного моделирования и экспериментальные подходы, изучили водные растворы соляной кислоты с низкими, средними и высокими концентрациями. В ходе исследования было обнаружено, что хлорид-анион и ион H+ остаются сближенными и формируют необычную структуру во всем диапазоне изученных концентраций.
Для изучения такого, казалось бы обычного объекта, как водные растворы соляной кислоты, исследователи из Тихоокеанской Северо-Западной Национальной лаборатории США использовали комбинацию метода рентгеновского поглощения, дифракции нейтронов и рентгеновской дифракции с моделированием методом функционала плотности. Говоря конкретнее, было измерено расстояние между хлорид-анионом и ионом гидроксония (эти ионы образуют тесную ионную пару), и было найдено, что расстояние хлор-кислород существенно меньше, чем предполагалось в рамках картины идеальной модели диссоциации.
Обнаруженные структуры значительно отличаются от структур, полученных при изучении газовой фазы, применявшихся для создания первичных расчетных моделей. В настоящий момент исследователи изучают растворы кислот уже не с точечными, а более сложными анионами, надеясь обнаружить для них специфическую картину взаимодействия гидроксоний-анион.
Источник: The Journal of Physical Chemistry B, 2014; 118 (26): 7211; DOI: 10.1021/jp501091h
О КОМПАНИИ
 ЗАО "Союзхимпром" более 15 лет работает в области комплексного оснащения химических и эколого-аналитических лабораторий, предприятий разного профиля, государственных служб охраны окружающей среды и санитарного контроля Урала, Сибири и Дальнего Востока.Все что Вам нужно. Основное преимущество новосибирского ЗАО "Союзхимпром" — комплексность поставки.
ЗАО "Союзхимпром" более 15 лет работает в области комплексного оснащения химических и эколого-аналитических лабораторий, предприятий разного профиля, государственных служб охраны окружающей среды и санитарного контроля Урала, Сибири и Дальнего Востока.Все что Вам нужно. Основное преимущество новосибирского ЗАО "Союзхимпром" — комплексность поставки.
КОНТАКТЫ
- 8-383-289-98-09; 289-98-08; 279-98-76; 279-97-52
- info.shp@yandex.ru
- shp-nsk
- 630015, Россия, Новосибирск, ул. Королева 40, корпус 87
Союзхимпром - лабораторное оборудование © 2024